Amila acetilsalikato
Aspekto
| Amila acetilsalikato | |
 | |
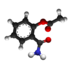
| Plata kemia strukturo de la Amila acetilsalikato | |
 | |
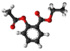
| Tridimensia kemia strukturo de la Amila acetilsalikato | |
| Kemia formulo | |
| Molmaso | 130,184g mol-1 |
(25 °C kaj 100 kPa) | |
Amila acetilsalikato, kemia formulo C4H18O4 estas organika reakciaĵo produktata per interago de la acetilsalikata acido kun amila alkoholo en ĉeesto de sulfata acido. Ĝi apartenas al la familio de la esteroj, do ĝi estas nesolvebla en akvo sed solvebla en organikaj solvantoj tiaj kiaj etanolo, kloroformo, benzeno, acetono, etero. ktp. Amila acetilsalikato estas uzata en organikaj sintezoj kaj en la fabrikado de farmaciaĵoj kaj kiel kemia reakciaĵo. Amila acetilsalikato reakcias kun fortaj oksidigagentoj kaj fortaj bazoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per traktado de acetilsalikata acido kaj amila alkoholo:
Sintezo 2
[redakti | redakti fonton]- Preparado per traktado de acetilsalikata anhidrido kaj amila alkoholo:
Sintezo 3
[redakti | redakti fonton]- Preparado per traktado de amila klorido kaj acetilsalikata acido:
Sintezo 4
[redakti | redakti fonton]- Preparado per interagado de fenila acetilsalikato kaj amila klorido:
Sintezo 5
[redakti | redakti fonton]- Preparado per transesterigo inter etila acetilsalikato kaj amila acetato:
Sintezo 6
[redakti | redakti fonton]- Preparado per acida transigo inter amila acetato kaj acetilsalikata acido:
Sintezo 7
[redakti | redakti fonton]- Preparado per alkohola transigo inter etila acetilsalikato kaj amila alkoholo:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Hidrolizo de la amila acetilsalikato:
Reakcio 2
[redakti | redakti fonton]- Sapigo de la amila acetilsalikato:
Reakcio 3
[redakti | redakti fonton]- Preparado per acida transigo inter amila acetilsalikato kaj acetata acido:
Reakcio 4
[redakti | redakti fonton]- Preparado per alkohola transigo inter amila acetilsalikato kaj etanolo:
Reakcio 5
[redakti | redakti fonton]- Reduktigo de la amila acetilsalikato:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun amoniako:
Reakcio 7
[redakti | redakti fonton]- Reakcio kun klorida acido:


![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)


![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{2[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3e0bf23d773dd68c0756bf7219ac82b7a51e73c6)