Cianoacetata acido
Aspekto
| Cianoacetata acido | ||||
 | ||||
| Plata kemia strukturo de la Cianoacetata acido | ||||
 | ||||
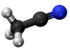
| Tridimensia kemia strukturo de la Cianoacetata acido | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 372-09-8 | |||
| ChemSpider kodo | 9357 | |||
| PubChem-kodo | 9740 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora aŭ flava, higroskopa solidaĵo | |||
| Molmaso | 85,062 g·mol-1 | |||
| Denseco | 1,287g cm−3 | |||
| Fandpunkto | 64 °C[1] | |||
| Bolpunkto | 108 °C[2] | |||
| Ekflama temperaturo | 107 °C | |||
| Solvebleco | Akvo:1000 g/L | |||
| Mortiga dozo (LD50) | 1500 mg/kg (buŝe) | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R22 R34 R52/53 [3] | |||
| Sekureco | S26 S36/37/39 S45 S61 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H302, H312, H314, H318, H332 | |||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P270, P271, P280, P301+312, P301+330+331, P303+361+353, P304+312, P304+340, P305+351+338, P310, P321, P330, P363, P405, P501[4] | |||
(25 °C kaj 100 kPa) | ||||
Cianoacetata acido aŭ C3H3NO2 estas kemia kombinaĵo, apartenanta al la funkcia grupo de la acidoj derivataj el interagado de la kloroacetata acido kaj natria cianido. Cianoacetata acido estas senkolora aŭ flava, higroskopa solidaĵo, uzata kiel analiza reakciaĵo en kemiaj sintezoj kaj en la fabrikado de kosmetikaĵoj kaj farmaciaĵoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per oksidado de la cianoetila alkoholo:
Sintezo 2
[redakti | redakti fonton]- Preparado per oksidigo de la cianoetanalo:
Sintezo 3
[redakti | redakti fonton]- Preparado per sapigo de la cianoacetila klorido:
Sintezo 4
[redakti | redakti fonton]- Preparado per hidratigo de la cianoacetila klorido:
Sintezo 5
[redakti | redakti fonton]- Preparado per sapigo de la cianoetanalo, sekvata per reakcio de la natria cianoacetato kun sulfata acido:[5]
Sintezo 6
[redakti | redakti fonton]- Preparado per interagado de la kloroacetata acido kaj natria cianido:
Sintezo 7
[redakti | redakti fonton]- Preparado per traktado de la sulfata acido sur cianoacetatoj:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Malkomponado de la cianoacetata acido:
Reakcio 2
[redakti | redakti fonton]- Metanola esterigo de la cianoacetata acido:
Reakcio 3
[redakti | redakti fonton]- Salformado per reakcio kun natria hidroksido:
Reakcio 4
[redakti | redakti fonton]- Preparado de la kloroacetata acido per interagado kun klorida acido:
Reakcio 5
[redakti | redakti fonton]- Preparado de la cianoacetamido:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun tionila klorido:
Reakcio 7
[redakti | redakti fonton]- Senhidratigo kun formado de la cianoacetata anhidrido en ĉeesto de fosfora kvinoksido:
Literaturo
[redakti | redakti fonton]- Science Direct
- Reag paperplane Arkivigite je 2018-07-31 per la retarkivo Wayback Machine
- Loba Chemie
- Chemicalland21
- Potentially Toxic and Hazardous Substances in the Industrial Organic Chemicals and Organic Dyes and Pigment Industries
- Name Reactions for Homologation
- Patty's toxicology
- Toxic substances control act
Referencoj
[redakti | redakti fonton]- ↑ Sigma Aldrich
- ↑ Chemical Book
- ↑ Merck Millipore[rompita ligilo]
- ↑ PubChem
- ↑ Link Springer






![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{2[O]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b3e1ba299ec9ffa6d9299ee90dc4b8e1bbb8d3f1)

![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{[O]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/83ec2f57b9a299cd8e6bda67656e3c78132275b1)

![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)
![{\displaystyle {\mathsf {{\xrightarrow[{H_{2}O}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c797066606e1ec973a46c67e24d1c0368934f8be)

![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{-H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/38ec2e343af3332af9f60a5bd305e77c6eaef1f4)