Etila glioksilato
Aspekto
| Etila glioksilato | |||
 | |||
| Bastona kemia strukturo de la Etila glioksilato | |||
 | |||
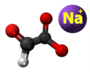
| Tridimensia kemia strukturo de la Etila glioksilato | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 924-44-7 | ||
| ChemSpider kodo | 63397 | ||
| PubChem-kodo | 70211 | ||
| Fizikaj proprecoj | |||
| Molmaso | 102,089 g·mol-1 | ||
| Denseco | 1,03g cm−3 | ||
| Bolpunkto | 110°C[1] | ||
| Refrakta indico | 1,475 | ||
| Ekflama temperaturo | 7 °C | ||
| Solvebleco | Akvo:Nesolvebla | ||
| Mortiga dozo (LD50) | 636 mg/kg (buŝe)[2] | ||
| Sekurecaj Indikoj | |||
| Riskoj | R11 R36/37/38 R48/20 R63 R65 R67 | ||
| Sekureco | S9 S16 S23 S24/25 S33 S36/37/39 S45 S60 S62 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H225, H304, H315, H333, H336, H361, H373 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P261, P264, P272, P280, P302+352, P303+361+353, P321, P332+313, P333+313, P362, P363, P370+378, P403+235, P501[3] | ||
(25 °C kaj 100 kPa) | |||
Etila glioksilato aŭ C4H6O3 estas kemia kombinaĵo, apartenanta al la funkcia grupo de la esteroj de la glioksilata acido kaj etanolo. Etila glioksilato estas alte brulema likvaĵo, uzata kiel kemia reakciaĵo en kemiaj sintezoj. Kutime ĝi estiĝas per kondensiĝa reakcio aŭ per esterigo de Fischer-Speyer kun sulfata acido kiel katalizilo. Etila glioksilato estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Etila glioksilato reakcias kun fortaj oksidigagentoj kaj fortaj bazoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per agado de glioksilata acido kaj etila alkoholo:
Sintezo 2
[redakti | redakti fonton]- Preparado per traktado de glioksilata anhidrido kaj etila alkoholo:
Sintezo 3
[redakti | redakti fonton]- Preparado per reakcio de etila klorido kaj glioksilata acido:
Sintezo 4
[redakti | redakti fonton]- Preparado per interagado de etila klorido kaj natria glioksilato:
Sintezo 5
[redakti | redakti fonton]- Preparado per transesterigo inter etila fenilacetato kaj fenetila glioksilato:
Sintezo 6
[redakti | redakti fonton]- Preparado per acida transesterigo inter etila cinamato kaj glioksilata acido:
Sintezo 7
[redakti | redakti fonton]- Preparado per alkohola transesterigo inter etila glioksilato kaj etila alkoholo:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Hidrolizo de la etila glioksilato:
Reakcio 2
[redakti | redakti fonton]- Sapigo de la etila glioksilato:
Reakcio 3
[redakti | redakti fonton]- Reakcio per acida transesterigo kun formiata acido:
Reakcio 4
[redakti | redakti fonton]- Reakcio per alkohola transesterigo kun benzila alkoholo:
Reakcio 5
[redakti | redakti fonton]- Reduktigo de la etila glioksilato:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun NH3:
Reakcio 7
[redakti | redakti fonton]- Reakcio kun HCl:
Literaturo
[redakti | redakti fonton]- Science Direct
- Drinking Water and Health
- Dictionary of Carbohydrates
- Fused Pyrimidines, Part 3: Pteridines
- Catalytic Asymmetric Friedel-Crafts Alkylations
- Asymmetric Catalysis on Industrial Scale: Challenges, Approaches and Solutions
- The chemical news
- Science of Synthesis: Houben-Weyl Methods of Molecular Transformations






![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)




![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{2[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3e0bf23d773dd68c0756bf7219ac82b7a51e73c6)
