Fenilsulfinata acido
Aspekto
| Benzenosulfinata acido | ||
 | ||
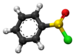
| Plata kemia strukturo de la Fenilsulfinata acido | ||
 | ||
| Tridimensia kemia strukturo de la Fenilsulfinata acido | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 618-41-7 | |
| ChemSpider kodo | 11560 | |
| PubChem-kodo | 12057 | |
| Fizikaj proprecoj | ||
| Aspekto | senkolora aŭ blanka higroskopa solidaĵo kun malalta fandpunkto | |
| Molmaso | 142,172−1 | |
| Denseco | 1,365g/cm−3[1] | |
| Fandpunkto | 84 °C | |
| Bolpunkto | 339.4 °C [2] | |
| Refrakta indico | 1,682[3] | |
| Ekflama temperaturo | 159,1 °C [4] | |
| Solvebleco | Akvo:0,955 g/L | |
| Mortiga dozo (LD50) | 1175 mg/kg (buŝe) [5] | |
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo-piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H302, H315, H319, H332, H335 | |
| GHS Deklaroj pri antaŭgardoj | P280, P305+351+338, P310 | |
(25 °C kaj 100 kPa) | ||
Fenilsulfinata acido estas senkolora aŭ blanka solidaĵo ĝenerale enstorigita sub ĝia formo de natria salo. En akva solvaĵo ĝi estas treege acida kaj facile oksidigebla sub la atmosfero. Ĝia produktado per interagado de la "fenilnatrio" kun sulfura duoksido estas konata ekde 1931.[6] Fenilsulfinataj acidoj reakcias kun sulfuro por doni tiosulfinatoj kaj tiosulfinataj acidoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per traktado de benzeno kaj sulfura duoksido:
Sintezo 2
[redakti | redakti fonton]- Preparado per traktado de benzenosulfinila klorido kaj natria hidroksido:
Sintezo 3
[redakti | redakti fonton]- Preparado per traktado de benzenosulfinila klorido kaj zinka hidroksido:
Sintezo 4
[redakti | redakti fonton]- Preparado per reduktado de benzenosulfonila klorido kun natria sulfito en akva medio:
Sintezo 5
[redakti | redakti fonton]- Preparado per traktado de natria benzenosulfinato kaj klorida acido:
Sintezo 6
[redakti | redakti fonton]- Preparado per acida interŝanĝo de fenila natrio kaj sulfura duoksido:
Sintezo 7
[redakti | redakti fonton]- Preparado per duobla interŝanĝo de fenila natrio kaj tionila klorido:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Sapigo de la fenilsulfinata acido
Reakcio 2
[redakti | redakti fonton]- Esterigo de la fenilsulfinata acido:
Reakcio 3
[redakti | redakti fonton]- Preparado de fenilsulfinilamido per acida interŝanĝo inter fenilsulfinata acido kaj amoniako:
Reakcio 4
[redakti | redakti fonton]- Preparado de klorosulfinata acido( CAS numero 25404-06-2 per alkohola interŝanĝo inter fenilsulfinata acido kaj kloro en acida medio:
Reakcio 5
[redakti | redakti fonton]- Klorigo de la fenilsulfinata acido:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun sodamido en acida medio:
Reakcio 7
[redakti | redakti fonton]- Reakcio kun nitrozila klorido:
Vidu ankaŭ
[redakti | redakti fonton]Referencoj
[redakti | redakti fonton]- ↑ Chemical Book
- ↑ Chemnet. Arkivita el la originalo je 2021-11-14. Alirita 2021-11-14 .
- ↑ Chembk
- ↑ Chemsrc
- ↑ Guidechem
- ↑ Organometallics in Synthesis





![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)




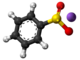

![{\displaystyle {\mathsf {{\xrightarrow[{-\;NaCl}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d203632e68b4407a833543c573208a5d632e2cdf)
![{\displaystyle {\mathsf {{\xrightarrow[{-\;HCl}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b9dba2fec3ed5be5edc819a4d2f1fa984d913593)


![{\displaystyle {\mathsf {{\xrightarrow[{}]{+[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/88fb0b03b975cfe42ff07b526c4bddf66812655c)


![{\displaystyle {\mathsf {{\xrightarrow[{}]{[OH]^{-}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/258ce3c08df9dce17beda55311dbfb79464c8a40)