p-Aminobenzoata acido
Aspekto
(Alidirektita el PABA)
| p-Aminobenzoata acido | ||
 | ||
| Plata kemia strukturo de la p-Aminobenzoata acido | ||
 | ||
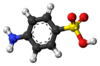
| Tridimensia kemia strukturo de la p-Aminobenzoata acido | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 150-13-0 | |
| ChemSpider kodo | 953 | |
| PubChem-kodo | 978 | |
| Merck Index | 15,418 | |
| Fizikaj proprecoj | ||
| Aspekto | blanka lumsensiva solidaĵo | |
| Molmaso | 137,138 g·mol-1 | |
| Denseco | 1,374g cm−3 | |
| Fandpunkto | 187°C-189°C[1] | |
| Bolpunkto | 339,9°C[2] | |
| Refrakta indico | 1,637 | |
| Ekflama temperaturo | 159,4 °C | |
| Acideco (pKa) | 4,98[3] | |
| Solvebleco | Akvo:4,7 g/L [4] | |
| Mortiga dozo (LD50) | 2850 mg/kg (buŝe) | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S36 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H302, H315, H317, H319 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P270, P271, P272, P280, P301+312, P302+352, P304+340, P305+351+338, P321, P330, P332+313, P333+313, P337+313, P362, P363, P403+233, P405, P501[5] | |
(25 °C kaj 100 kPa) | ||
p-Aminobenzoata acido aŭ C7H7NO2, ankaŭ konata kiel "PABA", estas organika kombinaĵo konsistante je unu fenila ringo ligita al unu amina radikalo kaj alia karboksilata acido. Ĝi estas blanka solidaĵo (malgraŭ ke la komercaj specimenoj povas esti brunaj aŭ flavecaj) malmulte solvebla en akvo kaj estas nature trovata en pluraj plantoj kaj manĝaĵoj. P-aminobenzoata acido estas uzata en farmakologio en la traktado de gastrointestaj simptomoj kaj kiel nutrosuplemento. Ferikaj saloj ĝin facile oksidigas, sed la flava koloro formita rapide ŝanĝiĝas je ruĝo per sunekspono. Aminobenzoata acido povas identigiĝi en la urino.
Sintezoj
[redakti | redakti fonton]Sintezo 1
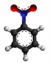
[redakti | redakti fonton]- Preparado ekde la nitrobenzeno per reduktado de la nitro-grupo kaj kataliza aldono de karbona duoksido:[6]
Sintezo 2
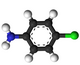
[redakti | redakti fonton]- Preparado ekde la anilino kaj kloroformiata acido:
Sintezo 3
[redakti | redakti fonton]- Preparado ekde la "kloroanilino" kaj natria formiato:
Sintezo 4
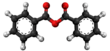
[redakti | redakti fonton]- Preparado ekde la benzoata anhidrido:
Sintezo 5
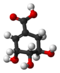
[redakti | redakti fonton]- Preparado ekde la "korismata acido":
Sintezo 6
[redakti | redakti fonton]- Preparado per reduktado de la "ŝikimata acido":
Sintezo 7
[redakti | redakti fonton]- Preparado ekde la "sulfanilata acido":
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Konvertado al nitrobenzeno:
Reakcio 2
[redakti | redakti fonton]- Konvertado al anilino:
Reakcio 3
[redakti | redakti fonton]- Konvertado al "p-kloroanilino":
Reakcio 4
[redakti | redakti fonton]- Konvertado al "fenazino" per senkarboksiligo de la aminobenzoataj acidoj sekvata per kataliza reduktigo de la anilinoj en ĉeesto de "plumba (II) oksido":[7]
Reakcio 5
[redakti | redakti fonton]- Konvertado al "korismata acido":
Reakcio 6
[redakti | redakti fonton]- Konvertado al "ŝikimata acido":
Reakcio 7
[redakti | redakti fonton]- Konvertado al "p-aminosulfanilata acido":
Vidu ankaŭ
[redakti | redakti fonton]Literaturo
[redakti | redakti fonton]- Science Direct
- Advances in 4-Aminobenzoic Acid Research and Application
- Taste Chemistry
- Fenaroli's Handbook of Flavor Ingredients
- Encyclopedia of Food and Color Additives
- Cinnamon and Cassia: The Genus Cinnamomum
- Aminobenzoic Acids—Advances in Research and Application
- RÖMPP Encyclopedia Natural Products




![{\displaystyle {\mathsf {{\xrightarrow[{LiAlH_{4}}]{+6[H]\,-2\,H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7b13016949cc7a7afb54c6ea289690d9005778cd)



![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)


![{\displaystyle {\mathsf {{\xrightarrow[{+2\,NH_{2}Cl}]{+H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f8c3eb4f83bd63678dd39653bd57f2a612e2c351)

![{\displaystyle {\mathsf {{\xrightarrow[{+NH_{2}Cl\,-HCl}]{+4[H]\,-H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b8ab35d42af78b7c9ae245d78fc4f71a9d31da9e)
![{\displaystyle {\mathsf {{\xrightarrow[{+NaNH_{2}\,-NaOH}]{+2[H]\,-2\,H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f1118be2ce8f45afe3f133803aeca6fc3eddc87f)
![{\displaystyle {\mathsf {{\xrightarrow[{+CO_{2}}]{-SO_{3}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7d25da64bfbe329643e8b56acd9fa0c4c563f91b)
![{\displaystyle {\mathsf {{\xrightarrow[{+KMnO_{4}\,-2\,H_{2}O}]{-CO_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9827dd9062184594a6994d565d6147c04584d666)

![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{-CO_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f7bf1d1bb277e0c1c24fb38c4d34882382b8e4bf)
![{\displaystyle {\mathsf {{\xrightarrow[{+Cl_{2}\,-HCl}]{-CO_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6fe126404d9362c982ab838f5a2ace68d8b3c25b)
![{\displaystyle {\mathsf {{\xrightarrow[{+PbO}]{-2\,CO_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5c6170ec17a94ca0ca7032a407598f3dcaee5706)

![{\displaystyle {\mathsf {{\xrightarrow[{-NaNH2\,-\,HCl}]{+NaOH}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eacf9efbfb384745d0889a5cbd65ef89cce8a39b)
![{\displaystyle {\mathsf {{\xrightarrow[{+2\,H_{2}O}]{+NaOH\,-NaNH2}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b4dfb384649550d83880ef6aa9c35a0065befe8f)
![{\displaystyle {\mathsf {{\xrightarrow[{+SO_{3}}]{-CO_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ba3a99d4b41a32bc6f4740cd1f909be990965977)