Trifluoro-acetata anhidrido
| Trifluoro-acetata anhidrido | |||
 | |||
| Plata kemia strukturo de la Trifluoro-acetata anhidrido | |||
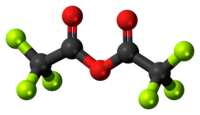 | |||
| Tridimensia kemia strukturo de la Trifluoro-acetata anhidrido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 407-25-0 | ||
| ChemSpider kodo | 21106178 | ||
| PubChem-kodo | 9845 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora, higroskopa likvaĵo kun penetranta odoro | ||
| Molmaso | 210,031 g·mol-1 | ||
| Denseco | 1,503g cm−3[1] | ||
| Fandpunkto | -63,5 °C | ||
| Bolpunkto | 40 °C | ||
| Refrakta indico | 1,2735 | ||
| Ekflama temperaturo | -26 °C[2] | ||
| Solvebleco | Akvo:reakcias | ||
| Mortiga dozo (LD50) | 200 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R14 R20 R35 R52/53 [3] | ||
| Sekureco | S8 S9 S26 S27 S28A S45 S61 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H314, H332, H412 | ||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P271, P273, P280, P301+330+331, P303+361+353, P304+312, P304+340, P305+351+338, P310, P312, P321, P363, P405, P501[4] | ||
(25 °C kaj 100 kPa) | |||
Trifluoro-acetata anhidrido aŭ C4F6O3 estas acida anhidrido de la trifluoro-acetata acido, senkolora, higroskopa likvaĵo kun penetranta odoro, fluora derivaĵo de la acetata anhidrido. Tiel kiel aliaj acidaj anhidridoj, ĝi uzatas por enkondukado de la koresponda trifluoroacetila grupo (F3C-C=OO-) en organikaj sintezoj.
Kvankam alte volatila (bolpunkto 39°C-40°C), trifluoro-acetata anhidrido estas pli konvena manipulado ol la koresponda acila klorido (bolpunkto -27 °C) aŭ la acila bromido (bolpunkto -5 °C). Trifluoro-acetata anhidrido plenumas gravan rolon en la fabrikado de vasta gamo da biologie aktivaj komponaĵoj por gaskromatografia analizo kaj kiel elsekigilo por trifluoro-acetata acido.
Ĝi same estas grava por oksidigo de aldehidoj en acidojn, esterojn, amidojn samkiel en la protektado de alkoholoj kaj aminoj. Krom tio, ĝi uzatas kiel analiza reakcianto, solvanto kaj senhidratiga kondensigagento. Ĝi servas kiel interaĵo en la produktado de fluoraj fajnaj kemiaĵoj, farmaciaĵoj kaj agrokemiaĵoj.
Trifluoro-acetata anhidrido estas la plej volatila kaj reakciema inter la anhidridoj kaj ĝi reakcias kun alkoholoj, aminoj kaj fenoloj. Ĝi estas miksebla kun benzeno, dukloro-metano, duetila etero, dumetil-formiamido, kvarhidro-furano kaj acetonitrilo. Trifluoro-acetata anhidrido estas uzata por esterigo de la kolesterolo.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per interagado de trifluoro-acetata acido kun fosfora kvinoksido:[5]
Sintezo 2
[redakti | redakti fonton]- Senhidratigo per sulfura trioksido:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Preparado de trifluoro-acetila klorido per interagado de tionila klorido kun trifluoro-acetata anhidrido:
Reakcio 2
[redakti | redakti fonton]- Preparado de 2,2,2-trifluoro-etanolo ekde la antaŭa reakcio. La klorido de trifluoro-acetilo antaŭe produktita reakcias kun klorida acido donante la deziratan substancon:
Reakcio 3
[redakti | redakti fonton]- Sintezo de natria trifluoroacetato per interagado de trifluoro-acetata anhidrido kaj natria hidroksido:
Literaturo
[redakti | redakti fonton]- Advances in Carbohydrate Chemistry
- Purification of Laboratory Chemicals
- Polyamic Acids and Polyimides: Synthesis, Transformations, and Structure
- The Peptides: Methods of Peptide Synthesis
- Pharmaceutical Manufacturing Encyclopedia
- Handbook of Food Analysis: Residues and other food component analysis
Referencoj
[redakti | redakti fonton]- ↑ Alfa Aesar
- ↑ Chemical Book
- ↑ Fisher Scientific[rompita ligilo]
- ↑ Pubchem
- ↑ Patents Google






![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)

![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)
![{\displaystyle {\mathsf {{\xrightarrow[{-SO_{2}}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7c1376b5312a5aa3ce4e994120c7182f3d18f204)