Tektorigenino
Aspekto
| Tektorigenino | ||
 | ||
| Plata kemia strukturo de la Tektorigenino | ||
 | ||
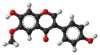
| Tridimensia kemia strukturo de la Tektorigenino | ||
 | ||
| Tektorigenino estas flava antioksidigaĵo trovata en plantoj tia kia la Pueraria thunbergiana[1] | ||
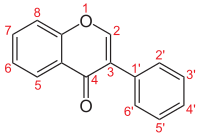 | ||
| Numerigo de la karbonaj strukturoj de la izoflavonoj. | ||
| Kemia formulo | ||
| CAS-numero-kodo | 548-77-6 | |
| ChemSpider kodo | 4445122 | |
| PubChem-kodo | 5281811 | |
| Merck Index | 15,9245 | |
| Fizikaj proprecoj | ||
| Aspekto | flava solidaĵo | |
| Molmaso | 300,263 g·mol−1 | |
| Denseco | 1,512g cm−3 | |
| Fandpunkto | 225 °C−226 °C[2] | |
| Bolpunkto | 601,5 °C[3] | |
| Refrakta indico | 1,697 | |
| Ekflama temperaturo | 230,1 °C | |
| Acideco (pKa) | 6,49 | |
| Solvebleco | Akvo:0,083 g/L [4] | |
| Mortiga dozo (LD50) | 300 mg/kg (buŝe)[5] | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S36 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H302 | |
| GHS Deklaroj pri antaŭgardoj | P264, P270, P301+312, P330, P501[6] | |
(25 °C kaj 100 kPa) | ||
Tektorigenino, (6-metokso,4',5,7-trihidrokso-izoflavono) aŭ C16H12O6 estas natura izoflavono, flava solidaĵo nesolvebla en akvo sed solvebla en etanolo, metanolo, kloroformo, acetono, duetila etero kaj acetatoj. Ĝi estas antiinflama,[7] antioksidiga,[8] antitumora[9] kaj antikancera[10] substanco kun sennombraj farmakologiaj aktivecoj. Tektorigenino estas nature trovata en sennombraj plantoj tiaj kiaj Pueraria thunbergiana, Iris unguicularis, kaj Belamcanda chinensis. Tektoridino estas la glukozido de la tektorigenino kun la samaj proprecoj.[11]
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado ekde la gliciteino per aldono de hidroksila grupo en la 5-a pozicio de la kromenonila grupo:
Sintezo 2
[redakti | redakti fonton]- Preparado ekde la irigenino per aldono de hidroksila grupo en la 3-a pozicio de la fenila grupo, interŝanĝo de la metoksila grupo je hidroksila grupo en la 4-a pozicio de la fenila grupo kaj forigo de metoksila grupo en la 5-a pozicio de la fenila grupo:
Sintezo 3
[redakti | redakti fonton]- Preparado ekde la kalikozino per aldono de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo kaj interŝanĝo de la metoksila grupo je hidroksila grupo en la 4-a pozicio de la fenila grupo:
Sintezo 4
[redakti | redakti fonton]- Preparado ekde la orobolo per aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, kaj forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo:
Sintezo 5
[redakti | redakti fonton]- Preparado ekde la pratenseino per aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo, kaj interŝanĝo de la metoksila grupo je hidroksila grupo en la 4-a pozicio de la fenila grupo:
Sintezo 6
[redakti | redakti fonton]- Preparado ekde la prunetino per aldono de metoksila grupo en la 6-a pozicio de la kromenonila grupo, interŝanĝo de la metoksila grupo je hidroksila grupo en la 7-a pozicio de la kromenonila grupo:
Sintezo 7
[redakti | redakti fonton]- Preparado per hidratigo de la tektoridino:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Konvertado al gliciteino per forigo de hidroksila grupo en la 5-a pozicio de la kromenonila grupo:
Reakcio 2
[redakti | redakti fonton]- Konvertado al irigenino per forigo de hidroksila grupo en la 3-a pozicio de la fenila grupo, interŝanĝo de la hidroksila grupo je metoksila grupo en la 4-a pozicio de la fenila grupo kaj aldono de metoksila grupo en la 5-a pozicio de la fenila grupo:
Reakcio 3
[redakti | redakti fonton]- Konvertado al kalikozino per forigo de hidroksila grupo en la 5-a pozicio de la kromenonila grupo, forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, aldono de hidroksila grupo en la 3-a pozicio de la fenila grupo kaj interŝanĝo de la hidroksila grupo je metoksila grupo en la 4-a pozicio de la fenila grupo:
Reakcio 4
[redakti | redakti fonton]- Konvertado al orobolo per forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, kaj aldono de hidroksila grupo en la 3-a pozicio de la fenila grupo:
Reakcio 5
[redakti | redakti fonton]- Konvertado al pratenseino per forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, aldono de hidroksila grupo en la 3-a pozicio de la fenila grupo, kaj interŝanĝo de la hidroksila grupo je metoksila grupo en la 4-a pozicio de la fenila grupo:
Reakcio 6
[redakti | redakti fonton]- Konvertado al prunetino per forigo de metoksila grupo en la 6-a pozicio de la kromenonila grupo, interŝanĝo de la hidroksila grupo je metoksila grupo en la 7-a pozicio de la kromenonila grupo:
Reakcio 7
[redakti | redakti fonton]- Konvertado al tektoridino:
Literaturo
[redakti | redakti fonton]- Traditional Medicines for Modern Times: Antidiabetic Plants
- Cancer Inhibitors from Chinese Natural Medicines
- Medicinal Plants in Asia for Metabolic Syndrome: Natural Products and ...
- Science Direct
- NCBI Resources
- Bio biologists
- Link Springer
- Encyclopedia of Traditional Chinese Medicines
Referencoj
[redakti | redakti fonton]- ↑ Traditional Medicines for Modern Times: Antidiabetic Plants
- ↑ Chemical Book
- ↑ Chemsrc
- ↑ FooDB
- ↑ Taylor & Francis online
- ↑ PubChem
- ↑ Psychopharmacology Bulletin
- ↑ Edible Medicinal and Non-Medicinal Plants
- ↑ Cancer Inhibitors from Chinese Natural Medicines
- ↑ Taxoids—Advances in Research and Application
- ↑ Cancer Inhibitors from Chinese Natural Medicines




![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)







![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{+H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/feea79f942bafc0daef2fb2f522afedc86391420)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{-H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/38ec2e343af3332af9f60a5bd305e77c6eaef1f4)