Radioaktiveco

Radioaktiveco estas la eco pri elsendo de subatomaj partikloj el atomkernoj.
Ĝi estas natura fenomeno, kiu spontanee okazas al kelkaj nuklidoj, nomataj radioaktivaj nuklidoj. La procezo ĝenerale ŝuldiĝas al la strukturo de la atomkerno, kiu povas havi eksceson de unu el la eroj (protonoj aŭ neŭtronoj) kiuj ĝin konsistigas.
La elsenditaj materialoj estas nomataj joniga radiado, kaj estas ĉefe de tri tipoj:
- Alfa-radiado: nukleoj de heliumo-4, elsenditaj nur de tre pezaj kernoj.
- Beta-radiado: elsendado de elektronoj je granda rapideco. Tio okazas ĝenerale ĉe kernoj kun eksceso de neŭtronoj, kiam unu el tiuj ĉi konvertiĝas en protonojn. Alia speco de beta-radiado estas la pozitiva beta-radiado, kiu konsistas en la elsendo de pozitronoj ĉe la transformado de protonoj en neŭtronojn.
- Gama-radiado: elsendo de elektromagneta radiado (fotonoj), akompanate al la elsendo de partikloj.
La rezultanta nukleo estas malsimila al la origina, kaj siavice povas esti ankaŭ radioaktiva, en kies kazo produktiĝas nova radioaktiva ĉeno.
Historio de malkovro
[redakti | redakti fonton]
Radioaktiveco estis malkovrita en 1896 fare de la Franca sciencisto Henri Becquerel, dum li estis laboranta ĉe fosforeskaj materialoj.[1] Tiuj materialoj brilis en malhelo post eksponado al lumo, kaj li suspektis, ke la brilo produktita en katodradia tubo pere de Ikso-radioj povus esti asociata kun fosforesko. Li envolvis fotografian platon en nigra papero kaj metis variajn fosforeskajn salojn en ĝin. Ĉiuj rezultoj estis negativaj ĝis li uzis salojn el uranio. La uranisaloj kreis nigrigon de la plato spite la fakton ke la plato jam estis envovlita en nigra papero. Tiuj radiadoj ricevis la nomon de "radioj de Becquerel".
Baldaŭ klariĝis, ke la nigrigo de la plato neniel rilatas al la fosforesko, ĉar la nigrigo estis produktita ankaŭ de ne-fosforeskaj saloj el uranio kaj eĉ de metala uranio mem. Klariĝis el tiuj eksperimentoj, ke estas formo de nevidebla radiado kiu povas trapasi tra papero kaj estis okaziginta la fakton ke la plato reagas kvazaŭ ĝi estas eksponita al la lumo.
Dekomence, aspektis, kvazaŭ tiu nova radioaktiveco estas simila al la tiam ĵus malkovritaj Ikso-radioj. Plia esplorado fare de Becquerel, Ernest Rutherford, Paul Villard, Pierre Curie, Marie Curie, kaj aliaj montris, ke tiu formo de radioaktiveco estas multe pli komplika. Rutherford estis la unua kiu konstatis, ke tiuj ĉiuj elementoj radias kongrue kun la sama matematika eksponencia formulo. Rutherford kaj lia disĉiplo Frederick Soddy estis la unuaj kiuj konstatis, ke multaj radiprocezoj rezultis en la transmutacio de unu elemento al alia. Poste, la leĝoj de radioaktiva transigo de Fajans kaj Soddy estis formulitaj por priskribi la produktojn de Alfa kaj Beta-radiado.[2][3]
La dekomencaj esploristoj malkovris ankaŭ, ke multaj aliaj kemiaj elementoj, krom uranio, havas radioaktivajn izotopojn. Sistema esplorado por la totala radioaktiveco en uraniaj ercoj gvidis ankaŭ la esploristojn Pierre kaj Marie Curie por izoligi du novajn elementojn: nome polonio kaj radiumo. Escepte pro la radioaktiveco de radiumo, la kemia simileco de radiumo al bario faris tiujn du elementojn malfacile distingeblaj.
La studoj de Marie kaj Pierre Curie pri radioaktiveco estas grava faktoro en scienco kaj medicino. Post ilia esplorado pri la radioj de Becquerel kondukis ilin al la malkovro kaj de la radiumo kaj de la polonio, ili stampis la terminon "radioaktiveco".[4] Ilia esplorado pri la penetrantaj radioj en uranio kaj la malkovro de radiumo lanĉis eraon de uzado de radiumo por la traktado de kancero. Ilia esplorado de radiumo povas esti konsiderita kiel la unua pacema uzado de nuklea energio kaj la startigo de moderna nuklea medicino.[4]
Dekomencaj sandanĝeroj
[redakti | redakti fonton]
La danĝeroj de Joniga radiado pro radioaktiveco kaj Ikso-radioj ne estis tuj agnoskitaj.
Ikso-radioj
[redakti | redakti fonton]La malkovro de Ikso-radioj fare de Wilhelm Röntgen en 1895 kondukis al disvastigita eksperimentado fare de sciencistoj, fizkistoj kaj inventistoj. Multaj personoj ekrakontis historiojn de bruligo, hararperdo kaj sanmalbonigo en teknikaj ĵurnaloj tiom frue kiom 1896. En februaro de tiu jaro, Profesoro Daniel kaj Dro. Dudley de Vanderbilt University plenumis eksperimenton pri ikso-radiado sur la kapo de Dudley kiu rezultis en lia hararperdo. Informo de Dro. H.D. Hawks, pri sia suferigaj akraj bruloj en mano kaj brusto dum montro de Ikso-radioj, estis la unua de multaj aliaj postaj informoj en Electrical Review.[5]
Ankaŭ aliaj eksperimentistoj, kiel Elihu Thomson kaj Nikola Tesla, informis pri bruligadoj. Thomson intence eksponis fingron al tubo de Ikso-radioj dum ioma periodo de tempo kaj suferis doloron, ŝveladon kaj brulegon.[6] Aliaj efikantoj, kiel ultraviola radiado kaj ozono, estis foje kulpigitaj pro la damaĝo,[7] kaj ankoraŭ multaj kuracistoj plendis, ke tio estas tute ne efiko de la ekspono al Ikso-radioj.[6]
Spite tion, estis kelkaj fruaj sistemaj kontraŭdanĝeraj esploroj, kaj tiom frue kiom ĝis en 1902 William Herbert Rollins verkis preskaŭ despere ke liaj avertoj pri la danĝeroj de la senzorga uzado de Ikso-radioj ne estis atentitaj, ĉu pere de industrio aŭ fare de siaj kolegoj. Tiame, Rollins estis pruvinta, ke la Ikso-radioj povas mortigi eksperimentajn animalojn, povas okazigi, ke graveda numido abortu, kaj ke tio povas mortigi abortaĵon.[8] Li ankaŭ rimarkis, ke "animaloj varias en la ricevo de ekstera agado de Ikso-radioj" kaj avertis, ke tiuj diferencoj estu konsiderataj kiam pacientoj estas traktataj pere de rimedoj de Ikso-radioj.
Radioaktivaj substancoj
[redakti | redakti fonton]
Tamen, la biologiaj efikoj de radiado pro radioaktivaj substancoj estis malfacile takseblaj. Tio havigis la oportunon por multaj kuracistoj kaj korporacioj merkatigi radioaktivajn substancojn kiel patentigitaj kuraciloj. Ekzemploj estas radiuma traktado per klistero, kaj radium-enhavaj akvoj trinkotaj kiel tonikaĵoj. Marie Curie protestis kontraŭ tiu speco de traktado, avertante, ke la efikoj de radiado sur la homa korpo ne estis bone komprenataj. Curie poste mortis pro aplazia anemio, plej verŝajne okazinta pro ekspono al joniga radiado. Ĉirkaŭ la 1930-aj jaroj, post nombraj okazoj de osta nekrozo kaj morto de entuziasmuloj de radiuma traktado, radium-enhavaj medicinaj produktoj estis forigitaj el la merkato (radioaktiva ĉarlatanismo).
Radiprotektado
[redakti | redakti fonton]Nur unu jaron post la malkovro fare de Röntgen pri la Ikso-radioj, la usona inĝeniero Wolfram Fuchs (1896) havigis tion kio estis probable la unua konsilo por protekto, sed nur en 1925 okazis la unua Internacia Kongreso de Radiologio (IKR) kaj ĝi konsideris la establadon de normigoj por internacia protektado. La efikoj de radiado sur genoj, inklude la efikon de kancera risko, estis agnoskitaj multe pli poste. En 1927, Hermann Joseph Muller publikigis esplorojn montrantajn genetikajn efikojn kaj, en 1946, li ricevis la Nobel-premion pri fiziologio aŭ medicino pro siaj trovitaĵoj.
La konsciiĝo de la potenciala danĝero, kiu havas la troan ekspozicion al la jonigaj radiadoj, kondukis la aŭtoritatojn fiksi la reglamentajn normojn por la limoj de dozo. Ĉi tiuj limoj respondas al suplementa risko akceptebla rilate al la natura risko.
Ekzemploj de radioaktivaj nuklidoj
[redakti | redakti fonton]
- Plutonio 239Pu kaj 241Pu
- Uranio 235U kaj 238U
- Kuriumo 242Cm kaj 244Cm
- Americio 241Am
- Torio 234Th
- Radiumo 242Cm
- Cezio 134Cs, 135Cs kaj 137Cs
- Jodo 129I, 131I kaj 133I
- Antimono 125Sb
- Rutenio 106Ru
- Stroncio 90Sr
- Kriptono 85Kr kaj 89Kr
- Seleno 75Se
- Kobalto 60Co
- Kloro 36Cl
- Karbono 14C
- Tritio 3H (radiaktiva hidrogeno)
Fizika unuo
[redakti | redakti fonton]
Radioaktiveco estas ankaŭ la nomo de fizika unuo, kiu mezuras la kvanton de radioaktiva materialo. Ĝi estas indikita per la nombro de malintegriĝoj en la unuo de tempo.
La SI unuo de radioaktiveco estas la bekerelo (simbolo Bq) kiu estas la derivita unuo pri radioaktiveco kadre de la Sistemo Internacia de Unuoj. Ĝi estas difinita kiel la aktiveco de kvanto de radioaktiva materio en kiu unu atoma nukleo diseriĝas en unu sekundo. Tial ĝi estas ekvivalenta al s−1. Oni povas ankaŭ uzi la bekerelon por la frekvenco de neperiodaj eventoj; por periodaj eventoj la herco, ankaŭ difinita kiel s−1, estas uzata kiel unuo.
Pli malnova unuo de radioaktiveco estis la kurio. Kurio estas ekvivalenta al 3,70 x 1010 diseriĝoj en unu sekundo: proksimume la aktiveco de 1 g de radiumo-226 (Ci), difinita kiel 3,7×1010 bekereloj aŭ 37 GBq.
Radioĥemio
[redakti | redakti fonton]
Radioĥemio estas la ĥemio de radioaktivaj materialoj, kie radioaktivaj izotopoj de elementoj uzatas por studi la ecojn kaj ĥemiajn reakciojn de ne-radioaktivaj izotopoj (ofte en radioĥemio la foresto de radioaktiveco kondukas al substanco priskribata kiel senaga kiam la izotopoj estas stabilaj). Ofte radioĥemiistoj traktas la uzon de radioaktiveco por studi ordinarajn ĥemiajn reakciojn.
Tipoj
[redakti | redakti fonton]Radioaktiva kadukiĝo rezultigas redukton de sumigita ripoz-maso, post kiam la liberigita energio (la disrompiĝinta energio) eskapis iel. Kvankam kadukiĝanta energio foje estas difinita kiel rilata al la diferenco inter la maso de la gepatraj nukleidproduktoj kaj la maso de la kadukigproduktoj, tio estas vera nur de ripozmasaj mezuradoj, en kiuj iom da energio estis forigita de la produktosistemo. Tio veras ĉar la disfala energio devas ĉiam porti mason kun si, kien ajn ĝi aperas laŭ la formulo E = mc2. La kadukiĝa energio estas komence liberigita kiel la energio de elsenditaj fotonoj plus la kineta energio de mas-elsenditaj partikloj (t.e., partikloj kiuj havas ripoz-mason). Se tiuj partikloj venas al termika ekvilibro kun sia medio kaj fotonoj estas absorbitaj, tiam la kadukiĝanta oenergio estas transformita al termika energio, kiu retenas sian mason.
Kadukiĝenergio, do, restas rilata al ia mezuro de la maso de la kaduksistemo, nomita senvaria maso, invarianta maso, ripoza maso aŭ simple maso, kiu ne ŝanĝiĝas dum la kadukiĝo, kvankam la energio de kadukiĝo estas distribuita inter kadukiĝpartikloj. La energio de fotonoj, la kinetika energio de elsenditaj partikloj, kaj, poste, la termika energio de la ĉirkaŭa materio, ĉiuj kontribuas al la invarianta maso de la sistemo. Tiel, kvankam la sumo de la ripozmasoj de la partikloj ne estas konservita en radioaktiva kadukiĝo, la sistema maso kaj sistema invarianta maso (kaj ankaŭ la sistema totalenergio) estas konservitaj dum ajna kadukprocezo. Ĉi tio estas konfirmo de la ekvivalentaj leĝoj de konservado de energio kaj konservado de maso.
Alfa, beta kaj gamma radiado
[redakti | redakti fonton]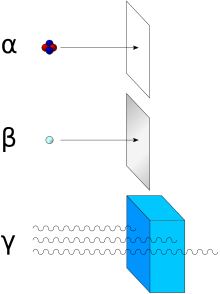
Fruaj esploristoj trovis, ke elektra aŭ magneta kampo povus dividi radioaktivajn elsendojn en tri specojn de radiadoj. La radioj ricevis la nomojn alfa, beta kaj gama, en kreskanta ordo de ilia kapablo penetri materion. Alfa-kadukiĝo estas observita nur en pli pezaj elementoj de atomnumero 52 (teluro) kaj pli granda, kun la escepto de berilio-8 (kiu kadukiĝas al du alfa-partikloj). La aliaj du specoj de kadukiĝo estas observataj en ĉiuj elementoj. Plumbo, atomnumero 82, estas la plej peza elemento kiu havas iujn ajn izotopojn stabilajn (ĝis la limo de mezurado) ĝis radioaktiva disfalo. Radioaktiva disfalo vidiĝas en ĉiuj izotopoj de ĉiuj elementoj de atomnumero 83 (bismuto) aŭ pli granda. Bismuto-209, tamen, estas nur tre iomete radioaktiva, kun duoniĝo de la tempo pli granda ol la aĝo de la universo; radioizotopoj kun ekstreme longaj duoniĝotempoj estas konsiderataj efike stabilaj por praktikaj celoj.
Analizante la naturon de la kadukiĝproduktoj, estis evidente de la direkto de la elektromagnetaj fortoj aplikitaj al la radiadoj per eksteraj magnetaj kaj elektraj kampoj ke alfa-partikloj portas pozitivan ŝargon, beta-partikloj portas negativan ŝargon, kaj gamaradioj estis neŭtralaj. De la grandeco de deflankiĝo, estis klare ke alfa-partikloj estis multe pli masivaj ol beta-partikloj. Pasi alfa-partiklojn tra tre maldika vitra fenestro kaj kapti ilin en senŝargiĝtubo permesis al esploristoj studi la Energia elsendospektron de la kaptitaj partikloj, kaj finfine pruvis, ke alfa-partikloj estas heliumaj kernoj. Aliaj eksperimentoj montris beta-radiadon, rezultiĝantan el kadukiĝo kaj katodradioj, estis altrapidaj elektronoj. Same, oni trovis, ke gama-radiado kaj Rentgenradioj estas talt-energia elektromagneta radiado.

Ankaŭ la rilato inter la tipoj de kadukiĝo komencis esti ekzamenita: ekzemple, gama-kadukiĝo preskaŭ estis trovita asociita kun aliaj specoj de kadukiĝo, kaj okazas proksimume en la sama tempo, aŭ poste. Gama kadukiĝo kiel aparta fenomeno, kun sia propra duoniĝotempo (nun nomita izomera transiro), estis trovita en natura radioaktiveco kiel rezulto de la gama-kadukiĝo de ekscititaj metastabilaj atomizomeroj, kiuj estis en victurno kreitaj de aliaj specoj de kadukiĝo. Kvankam alfa, beta, kaj gama radiadoj estis plej ofte trovitaj, aliaj tipoj de elsendado estis poste malkovritaj. Baldaŭ post la eltrovo de la pozitrono en kosmaradiaj produktoj, estis ekkomprenite ke la sama procezo kiu funkcias en klasika beta-disfalo ankaŭ povas produkti pozitronojn (pozitronelsendo), kune kun neŭtrinoj (klasika beta-disfalo produktas antineŭtrinojn).
Elektronkapto
[redakti | redakti fonton]En elektronkapto, oni trovis, ke kelkaj proton-riĉaj nukleidoj kaptas siajn proprajn atomelektronojn anstataŭ elsendi pozitronojn, kaj poste, tiuj nukleidoj elsendas nur neŭtrinon kaj gamaradion de la ekscitita nukleo (kaj ofte ankaŭ Auger-elektronojn kaj karakterizajn Ikso-radiojn, kiel rezulto de la misordigo de elektronoj por plenigi la lokon de la perditaj kaptitaj elektronoj). Tiuj tipoj de kadukiĝo implikas la atomkapton de elektronoj aŭ elsedon de elektronoj aŭ pozitronoj, kaj tiel agas por movi nukleon direkte al la rilatumo de neŭtronoj al protonoj, kiu havas la malplej grandan kvanton da energio por antaŭfiksita tutsumo de nukleonoj. Tio sekve produktas pli stabilan (pli malaltan energion) nukleon.
Hipoteza procezo de pozitrona kapto, analoga al elektrona kapto, estas teorie ebla en kontraŭmateriaj atomoj, sed ne estis observita, ĉar kompleksaj kontraŭmateriaj atomoj preter kontraŭheliumo ne estas eksperimente haveblaj.[9] Tia kadukiĝo postulus kontraŭmateriajn atomojn almenaŭ same kompleksajn kiel berilio-7, kiu estas la plej malpeza konata izotopo de normala materio por sperti kadukiĝon per elektrona kapto.[10]
Nukle-elsendo
[redakti | redakti fonton]
Baldaŭ post la eltrovo de la neŭtrono en 1932, Enrico Fermi ekkomprenis, ke kelkaj maloftaj beta-kadukaj reagoj tuj donas neŭtronojn kiel kroma kadukiĝ-partiklo, tiel nomita beta-malfrua neŭtrona elsendo. Neŭtronelsendo kutime okazas el nukleoj, kiuj estas en ekscitita stato, kiel ekzemple la ekscitita 17O* produktita de la beta-disfalo de 17N. La neŭtrona elsendoprocezo mem estas kontrolita fare de la atomforto kaj tial estas ekstreme rapida, foje referencita kiel "preskaŭ tuja". Izolita protonelsendado estis poste observita en kelkaj elementoj. Oni trovis ankaŭ, ke kelkaj pezaj elementoj povas sperti spontanean fision en produktoj kiuj varias laŭ kunmetaĵo. En fenomeno nomita grapolkadukiĝo, oni trovis, ke specifaj kombinaĵoj de neŭtronoj kaj protonoj krom alfa-partikloj (heliumnukleoj) estis spontanee elsenditaj de atomoj.
Pli ekzotaj tipoj de radioaktiveco
[redakti | redakti fonton]Aliaj tipoj de radioaktiva disfalo estis trovitaj elsendi antaŭe viditajn partiklojn sed per malsamaj mekanismoj. Ekzemplo estas interna konvertiĝo, kiu rezultigas komencan elektron-elsedon, kaj poste ofte pliajn karakterizajn Ikso-radiojn kaj Auger-elektronan elsendadon, kvankam la interna konverta procezo implikas nek beta-n nek gama-kadukiĝon. Neŭtrino ne estas elsendita, kaj neniu el la elektrono(j) kaj fotono(j) elsenditaj originiĝas en la nukleo, kvankam la energio por elsendi ĉiujn ja originas tie. Interna konverta kadukiĝo, kiel izomera transirgama kadukiĝo kaj neŭtronelsendado, implikas la liberigon de energio de ekscitita nukleido, sen la transmutacio de unu elemento en alian.
Maloftaj okazaĵoj kiuj implikas kombinaĵon de du beta-kadukiĝ-specaj okazaĵoj okazantaj samtempe estas konataj (vidu malsupre). Ĉiu kadukiĝ-procezo, kiu ne malobservas la konservadon de energio aŭ impetleĝoj (kaj eble aliaj partiklokonservadaj leĝoj) povas okazi, kvankam ne ĉiuj estis detektitaj. Interesa ekzemplo studita finfine, estas ligo de la stato de beta-disfalo de renio-187. En ĉi tiu procezo, la beta-elektron-kadukiĝo de la gepatronukleido ne estas akompanata per beta-elektronelsendado, ĉar la beta-partiklo estis kaptita en la K-ŝelon de la elsenda atomo. Kontraŭneŭtrino estas elsendita, kiel en ĉiuj negativaj beta-disfaloj.
Se energicirkonstancoj estas favoraj, antaŭfiksita radionukleido povas trairi multajn konkurantajn specojn de kadukiĝo, kaj kelkaj atomoj kadukiĝas per unu vojo, dum aliaj kadukiĝas per alia. Ekzemplo estas kupro-64, kiu havas 29 protonojn, kaj 35 neŭtronojn, kiu kadukiĝas pro duoniĝotempo de 12,7004(13) horoj.[11] Tiu izotopo havas unu neparigitan protonon kaj unu neparigitan neŭtronon, do aŭ la protono aŭ la neŭtrono povas kadukiĝi al la alia partiklo, kiu havas kontraŭan izospinon. Tiu ĉi speciala nukleido (kvankam ne ĉiuj nukleidoj en ĉi tiu situacio) pli verŝajne disfalos per beta plus disfalo (61.52(26)%[11]) ol per elektrona kapto (38.48(26)%[11]). La ekscititaj energistatoj rezultiĝantaj el tiuj kadukiĝoj kiuj malsukcesas finiĝi en grundenergia stato, ankaŭ produktas pli postan internan konvertiĝon kaj gama-kadukiĝon en preskaŭ 0.5% de la tempo.
Kadukĉenoj kaj pluraj manieroj
[redakti | redakti fonton]
La fil-nukleido de kadukiĝokazaĵo ankaŭ povas esti malstabila (radioaktiva). En ĉi tiu kazo, ĝi ankaŭ kadukiĝos, produktante radiadon. La rezulta dua fil-nukleido ankaŭ povas esti radioaktiva. Tio povas konduki al sekvenco de pluraj kadukiĝokazaĵoj nomitaj kaduk-ĉeno (vidu artikolon por specifaj detaloj de gravaj naturaj kaduk-ĉenoj). Poste, stabila nukleido estas produktita. Ĉiuj kadukiĝintaj rezultoj, kiuj estas la rezulto de alfa-kadukiĝo, ankaŭ rezultigos heliumajn atomojn.
Kelkaj radionukleidoj povas havi plurajn malsamajn vojojn de kadukiĝo. Ekzemple, 35.94(6)%[11] de bismuto-212 kadukiĝas, tra alfa-elsendo, al taliumo-208 dum 64.06(6)%[11] de bismuto-212 kadukiĝas, tra beta-elsendo, al polonio-212. Kaj taliumo-208 kaj polonio-212 estas radioaktivaj fil-produktoj de bismuto-212, kaj ambaŭ kadukiĝas rekte al stabila plumbo-208.
Ekzistado kaj aplikoj
[redakti | redakti fonton]Laŭ la teorio de Praeksplodo, stabilaj izotopoj de la plej malpezaj tri elementoj (H, He, kaj spuroj de Li) estis produktitaj tre baldaŭ post la apero de la universo, en procezo nomita Praeksploda nukleosintezo. Tiuj plej malpezaj stabilaj nukleidoj (inkluzive de deŭterio) pluvivas ĝis nun, sed ĉiuj radioaktivaj izotopoj de la malpezaj elementoj produktitaj en la Praeksplodo (kiel ekzemple tricio) delonge kadukiĝis. Izotopoj de elementoj pli pezaj ol boro ne estis produktitaj en la Praeksplodo, kaj tiuj unuaj kvin elementoj ne havas iujn ajn longvivajn radioizotopojn. Tiel, ĉiuj radioaktivaj nukleoj estas, do, relative junaj kun rilato al la naskiĝo de la universo, formiĝis poste en diversaj aliaj specoj de nukleosintezo en steloj (aparte, supernovaoj), kaj ankaŭ dum daŭrantaj interagoj inter stabilaj izotopoj kaj energiaj partikloj. Ekzemple, karbono-14, radioaktiva nukleido kun duoniĝotempo de nur 5700 (30) jaroj,[11] estas konstante produktita en la supra atmosfero de la Tero pro interagoj inter kosmaj radioj kaj nitrogeno.
Nukleidoj kiuj estas produktitaj per radioaktiva disfalo estas nomitaj radiogenaj nukleidoj, ĉu ili mem estas stabilaj aŭ ne. Ekzistas stabilaj radiogenaj nukleidoj kiuj estis formitaj de mallongdaŭraj formortintaj radionukleidoj en la frua Sunsistemo.[12][13] La ekstra ĉeesto de tiuj stabilaj radiogenaj nukleidoj (kiel ekzemple ksenono-129 de formortinta jodo-129) kontraŭ la fono de praaj stabilaj nukleidoj povas esti konkludita per diversaj rimedoj.
Radioaktiva kadukiĝo estis uzata en la tekniko de radioizotopa etikedado, kiu kutimas spuri la trairejon de kemia substanco tra kompleksa sistemo (kiel ekzemple vivanta organismo). Provaĵo de la substanco estas sintezita kun alta koncentriĝo de malstabilaj atomoj. La ĉeesto de la substanco en unu aŭ alia parto de la sistemo estas determinita detektante la lokojn de kadukiĝ-okazaĵoj.
Sur la kondiĉo ke radioaktiva kadukiĝo estas vere hazarda (prefere ol simple ĥaosa), ĝi estis uzita en aparataraj hazard-nombraj generatoroj. Ĉar la procezo supozeble ne varias signife laŭ mekanismo dum la tempopaso, ĝi ankaŭ estas valora ilo en taksado de la absolutaj aĝoj de difinitaj materialoj. Por geologiaj materialoj, la radioizotopoj kaj kelkaj el siaj kaduk-produktoj iĝas kaptitaj kiam roko solidiĝas, kaj tiam povas poste esti uzitaj (kondiĉigita de multaj bonkonataj kvalifikoj) por taksi la daton de la solidiĝo. Ĉi tio inkluzivas kontroli la rezultojn de pluraj samtempaj procezoj kaj iliajn produktojn unu kontraŭ la alia, ene de la sama specimeno. Simile, kaj ankaŭ kondiĉigita de kvalifiko, la indico de formado de karbono-14 en diversaj epokoj, povas taksi la daton de formado de organika materio ene de preciza periodo rilata al la duoniĝotempo de la izotopo, ĉar la karbono-14 iĝas kaptita kiam la organika materio kreskas kaj asimilas la novan karbonon-14 de la aero. Poste, la kvanto de karbono-14 en organika materio malpliiĝas laŭ kadukiĝoprocezoj kiuj ankaŭ povas esti sendepende kruckontrolitaj per aliaj rimedoj (kiel ekzemple kontrolado de la karbono-14 en individuaj arboringoj, ekzemple).
Radioaktiva rubo
[redakti | redakti fonton]
Radioaktiva rubo estas materialo, kiu havas radioaktivajn ecojn kaj kiu ne havas pluan valoran eluzon.
Oni kutime dividas la rubon laŭ sia aktiveco jene:
- malaltaktivaj – kutime restaĵoj de malmulte kontaminitaj materialoj
- meze aktivaj – pluraj kontaminitaj materialoj kun pli granda enhavo, laŭ speco eblas deponi en supraĵan aŭ profundan deponejon
- alte aktivaj – ekzemple forbrulinta nuklea bruligaĵo aŭ restaĵoj post ties alilaborigo
Laŭ deveno de la rubo oni eblas dividi ĝin jene:
- Forbrulinta nuklea bruligaĵo – kiu estas deponata post eluzo en nukleja elektrejo kaj poste ĝi estas deponita en ŝirmajn kontenerojn en subterejo. Fakte ne temas pri absoluta rubo, ĉar eblas ties plua eluzo.
- Restaĵoj el diagnostiko en sansistemo – restinta materialo el sansistemo uzita dum diagnostiko aŭ dum kuracado de malsanoj – radiologio (ekz.: gama tranĉilo)
Institucioj
[redakti | redakti fonton]Gravuloj
[redakti | redakti fonton]Vidu ankaŭ
[redakti | redakti fonton]- Atombombo
- Atomeksplodo
- Atomkerno
- Izotopo
- Radionuklido
- Kalkulilo Geiger
- Nuklea izomero
- Partikla radiado
- Radiobiologio
- Radiologio
Referencoj
[redakti | redakti fonton]- ↑ Mould, Richard F.. (1995) A century of X-rays and radioactivity in medicine : with emphasis on photographic records of the early years, ‑a eldono, Bristol: Inst. of Physics Publ., p. 12. ISBN 978-0-7503-0224-1.
- ↑ Kasimir Fajans, "Radioactive transformations and the periodic system of the elements". Berichte der Deutschen Chemischen Gesellschaft, Nr. 46, 1913, pp. 422–439
- ↑ Frederick Soddy, "The Radio Elements and the Periodic Law", Chem. News, Nr. 107, 1913, pp. 97–99
- ↑ 4,0 4,1 L'Annunziata, Michael F.. (2007) Radioactivity: Introduction and History. Amsterdam, Netherlands: Elsevier Science, p. 2. ISBN 9780080548883.
- ↑ (2011) “Early victims of X-rays: a tribute and current perception”, Dentomaxillofacial Radiology 40 (2), p. 123–125. doi:10.1259/dmfr/73488299.
- ↑ 6,0 6,1 Ronald L. Kathern kaj Paul L. Ziemer, The First Fifty Years of Radiation Protection, physics.isu.edu. Arkivita el la originalo je 2017-09-12. Alirita 2019-10-07 .
- ↑ (July 2008) “Nikola Tesla and the Discovery of X-rays”, RadioGraphics 28 (4), p. 1189–92. doi:10.1148/rg.284075206.
- ↑ Geoff Meggitt (2008), Taming the Rays - A history of Radiation and Protection., Lulu.com, (ISBN 978-1-4092-4667-1)
- ↑ Radioactive Decay. Alirita 2022-05-05 .
- ↑ CH103 – Chapter 3: Radioactivity and Nuclear Chemistry – Chemistry (en-US). Alirita 2022-07-05 .
- ↑ 11,0 11,1 11,2 11,3 11,4 11,5 Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties" (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ↑ Clayton, Donald D.. (1983) Principles of Stellar Evolution and Nucleosynthesis, 2‑a eldono, University of Chicago Press. ISBN 978-0-226-10953-4.
- ↑ John H. Reynolds, Physics: Berkeley. The University of California, Berkeley (2007). Alirita 2007-10-01 .
- En tiu ĉi artikolo estas uzita traduko de teksto el vikipedia artikolo Radioactive decay angle.

