Furfurilamino
Aspekto
| Bonvolu ne konfuzi... | |
 |
 |
| Ili apartenas al du malsimilaj funkciaj grupoj, la unua estas amino de la metilfurano, pli konata kiel furfurilo, la dua estas amido de la metilfuranila grupo. | |
| 2-Furfurilamino | |||
 | |||
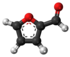
| Plata kemia strukturo de la Furfurilamino | |||
 | |||
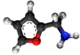
| Tridimensia kemia strukturo de la Furfurilamino | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 617-89-0 | ||
| ChemSpider kodo | 3320 | ||
| PubChem-kodo | 3438 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora aŭ flava likvaĵo | ||
| Molmaso | 97,117 g·mol−1 | ||
| Denseco | 1,099g cm−3 | ||
| Fandpunkto | -70 °C[1] | ||
| Bolpunkto | 145 °C[2] | ||
| Refrakta indico | 1,4886 | ||
| Ekflama temperaturo | 37 °C | ||
| Memsparka temperaturo | 350 °C[3] | ||
| Solvebleco | Akvo:Tute solvebla | ||
| Mortiga dozo (LD50) | 200 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R10 R36/37/38 [4] | ||
| Sekureco | S16 S23 S24/25 S26 S36/37/39 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H226, H301, H302, H310, H311, H312, H314, H332 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P260, P261, P262, P264, P270, P271, P280, P301+310, P301+312, P301+330+331, P302+352, P303+361+353, P304+312, P304+340, P305+351+338, P310, P321, P330, P361, P363, P370+378, P403+235, P405, P501[5] | ||
(25 °C kaj 100 kPa) | |||
Furfurilamino aŭ C5H7NO estas kemia kombinaĵo, apartenanta al la funkcia grupo de la primaraj ciklaj aminoj, rezultanta el interagado de la furfuralo kaj amoniako. Ĝi estas senkolora aŭ flava likvaĵo kun odoro je fiŝo kaj antibakteriaj kaj antikorodaj proprecoj uzata kiel kemia reakciaĵo kaj en la produktado de farmaciaĵoj. Tiel kiel la amoniako, furfurilamino estas malforta bazo kaj reakcias kun acidoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per interagado de furfuralo kaj amoniako:
Sintezo 2
[redakti | redakti fonton]- Preparado per interagado de furfurila alkoholo kaj amoniako:
Sintezo 3
[redakti | redakti fonton]- Preparado per interagado de furfurila klorido kaj amoniako:
Sintezo 4
[redakti | redakti fonton]- Preparado per reduktigo de la furfurilamido:
Sintezo 5
[redakti | redakti fonton]- Preparado per reduktigo de la furanonitrilo:
Sintezo 6
[redakti | redakti fonton]- Preparado per interagado de la metilfurano kaj ureo en alkala medio:
Sintezo 7
[redakti | redakti fonton]- Preparado per rearanĝo de Curtius:[6]
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Hidrolizo de la furfurilamino:
Reakcio 2
[redakti | redakti fonton]- Sapigo de la furfurilamino:
Reakcio 3
[redakti | redakti fonton]Reakcio 4
[redakti | redakti fonton]Reakcio 5
[redakti | redakti fonton]- Reakcio kun HNO2:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun HNCO:
Reakcio 7
[redakti | redakti fonton]- Reakcio kun acetila klorido:
Literaturo
[redakti | redakti fonton]- The Good Scents Company
- Fisher Scientific
- CDH Fine Chemical Arkivigite je 2019-04-04 per la retarkivo Wayback Machine
- World Scientific
- Advanced and Emerging Polybenzoxazine Science and Technology
- Production of Biofuels and Chemicals with Bifunctional Catalysts
- Toxic substances control act
- Russian Journal of Electrochemistry
Referencoj
[redakti | redakti fonton]- ↑ Chemical Book
- ↑ Sigma Aldrich
- ↑ LobaChemie
- ↑ NW Missouri Arkivigite je 2014-09-26 per la retarkivo Wayback Machine
- ↑ PubChem
- ↑ Chemistry LibreTexts
- ↑ ACS Publications






![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)

![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{2[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3e0bf23d773dd68c0756bf7219ac82b7a51e73c6)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{4[H]}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0e0b269271413ecc4960db8a3b5b06d3d74469e7)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{OH^{-}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8ac0ccd1160ee2589b80d8bc66b15c301af7f06e)
![{\displaystyle {\mathsf {{\xrightarrow[{-NaCl}]{-N_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/159ab497ad7e142d3bd54077269b13d91912fdb3)
![{\displaystyle {\mathsf {{\xrightarrow[{-CO_{2}}]{+H_{2}O}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2a3b277e66714c91147a6c2a2ccc0734102f5a31)

![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)
