Amonia pirosulfito
| Amonia pirosulfito | |||
  
| |||
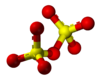
| Kemia strukturo de la Amonia pirosulfito | |||
| |||
| Kemia strukturo de la Amonia pirosulfito | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 10031-68-2 | ||
| ChemSpider kodo | 10219678 | ||
| Fizikaj proprecoj | |||
| Molmaso | 180.20392 g mol−1 | ||
| Smiles | [NH4+].[NH4+].[O-]S(=O)S(=O)(=O)[O-] | ||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H290, H314, H318, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P260, P264, P271, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P363, P391, P403, P405, P406, P501 | ||
(25 °C kaj 100 kPa) | |||
Amonia pirosulfito, pirosulfito de amonio aŭ (NH4)2S2O5 estas neorganika salo rezultanta el reakcio inter la amoniako kaj pirosulfita acido. La strukturo de la amonia pirosulfito estis starigita de argentina kemiisto Sergio Baggio, en 1971. En tiu sama jaro, Scargill mezuris la dissocigan varmon de la amonia sulfido kaj amonia dusulfito, kaj raportis ke la ĉeesto de humideco en la aero favoras la sulfitan estigon, dum nur akvo favoras produktadon de pirosulfato[1].
Sintezoj
[redakti | redakti fonton]Amonia pirosulfito estiĝas per termika dumerizado de la amonia bisulfito kun akvoforigo:
aŭ per reakcio de amonia sulfito kaj sulfura duoksido:
Titov (1983) studis miksaĵon da sulfura duoksido, amoniako kaj akvo kun estiĝo de amonia pirosulfito.
Tamen, ĉi-miksaĵo estigas amonian sulfiton[2] sub pli altaj temperaturoj:
Reakcio
[redakti | redakti fonton]Pirosulfito de amonio reakcias kun klorida acido estigante sulfuran duoksidon kaj amonia klorido
Literaturo
[redakti | redakti fonton]- Sulfites, Selenites & Tellurites[rompita ligilo], M.R. Masson,H.D. Lutz,B. Engelen
- Sulfur, Energy, and Environment, Beat Meyer
- ResearchGate
- Exploring Venus as a Terrestrial Planet, Larry W. Esposito,Ellen R. Stofan,Thomas E. Cravens
- Nonaqueous Electrolytes Handbook, Volume 2, G.J. Janz
- Literature 1985, Parte 1, S. Böhme, U. Esser, Prof. Dr. W. Fricke, H. Hefele, Inge Heinrich, W. Hofmann, R. Krahn, V. R. Matas, Dr. Lutz D. Schmadel, G. Zech
Referencoj
[redakti | redakti fonton]- ↑ Sulfur, Energy, and Environment, Beat Meyer
- ↑ Photochemistry of the Atmospheres of Mars and Venus, Vladimir A. Krasnopolsky
| ||||||








