Kalia ferocianido
| Kalia ferocianido | ||
 | ||
| Plata kemia strukturo de la Kalia ferocianido | ||
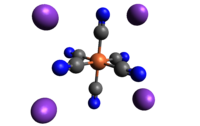 | ||
| Tridimensia kemia strukturo de la Kalia ferocianido | ||
 | ||
| Flavecaj kristaloj de kalia ferocianido. | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 13943-58-3 | |
| ChemSpider kodo | 7879375 | |
| PubChem-kodo | 11963580 11963580 | |
| Fizikaj proprecoj | ||
| Aspekto | klarflava solidaĵo | |
| Molmaso | 368346 g·mol−1 | |
| Denseco | 1.850g cm−3 | |
| Fandpunkto | 70 °C | |
| Bolpunkto | 650 °C | |
| Solvebleco | Akvo:289 g/L | |
| Mortiga dozo (LD50) | 6400 mg/kg (buŝe) | |
| Sekurecaj Indikoj | ||
| Riskoj | R32 R52 R53 [1] | |
| Sekureco | S50 S61 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H302, H312, H315, H319, H332, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P270, P271, P280, P301+312, P302+352, P304+312, P304+340, P305+351+338, P312, P321, P330, P332+313, P337+313, P362, P363, P403+233, P405 | |
(25 °C kaj 100 kPa) | ||
Kalia ferocianido estas neorganika kombinaĵo, lemon-kolora solidaĵo rezultanta el interagado de la ferocianida acido kaj kalia hidroksido. Ferocianido de kalio produktas blukoloron kiam ĝi reakcias kun ferikaj derivaĵoj. Kiam ĝi reakcias kun feroza salo la precipitaĵo estas blanka. Kalia ferocianido trovas multajn uzojn kaj aplikojn en industrio. Ĝi uzatas por purigado de stano kaj apartigo de la kupro elde molibdenaj ercoj. Ĝi ankaŭ estas uzata en la produktado de vino kaj citrata acido.
En laboratorio, kalia ferocianido estas uzata por determini la koncentriĝon de kalia permanganato, komponaĵo ofte uzata en titradoj surbaze de redoksaj reakcioj. Kalia ferocianido povas esti uzata kiel sterko por plantoj. Antaŭ la 19-a jarcento, kalia ferocianido estis la plej grava fonto de produktado je alkalo-metalaj cianidoj. Laŭ ĉi-historia procezo, kalia cianido estis produktita per malkomponado de la kalia ferocianido.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Kalia ferocianido estas preparebla en du etapoj: unue, reakciante cianidan acidon kun feroza klorido kaj kalcia hidroksido. La sekvan etapon oni interagas la kalcian ferocianidon formitan kun kalia karbonato:
|
|
Sintezo 2
[redakti | redakti fonton]- Alia preparado estas reakciigi cianidan acidon kun feroza klorido kaj poste aldoni kalian hidroksidon por neŭtraligi la solvaĵon:
|
|
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]|
|
Reakcio 2
[redakti | redakti fonton]- Pirolizo de la kalia ferocianido donas feran karbidon:
|
|
Reakcio 3
[redakti | redakti fonton]- Per sulfata acido, kalia ferocianido reakcias estigante sulfatojn kaj karbonan unuoksidon:
|
|
Reakcio 4
[redakti | redakti fonton]- En acida medio, kalia ferocianido reakcias kun kalia permanganato estigante sulfatojn kaj karbonan duoksidon:
|
|
Reakcio 5
[redakti | redakti fonton]- Kalia ferocianido reakcias kun arĝenta nitrato estigante blankan precipitaĵon de arĝenta ferocianido kaj kalia nitrato:
|
|
Reakcio 6
[redakti | redakti fonton]- Kalia ferocianido reakcias kun kupra sulfato por produkti brunan precipitaĵon de kupra ferocianido:
|
|
Reakcio 7
[redakti | redakti fonton]- Kalia ferocianido reakcias kun ferika klorido por doni bluan precipitaĵon de ferika ferocianido kaj kalia klorido:
|
|
Literaturo
[redakti | redakti fonton]- YSI
- Fisher Scientific Arkivigite je 2020-11-12 per la retarkivo Wayback Machine
- LabChem[rompita ligilo]
- Food Additives in Europe 2000
- Connaissance Et Travail Du Vin
- Diazo Chemistry - Synthesis and Reactions
Referencoj
[redakti | redakti fonton]
| ||||||



![{\displaystyle {6\,HCN+FeCl_{2}+2\,Ca(OH)2{\xrightarrow[{}]{T}}Ca_{2}[Fe(CN)_{6}]+4\,H_{2}O+2\,HCl}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b7be318d368a0230fbe244bcfaea7157d32a4408)
![{\displaystyle {Ca_{2}[Fe(CN)_{6}]+2\,K_{2}CO_{3}{\xrightarrow[{}]{T}}K_{4}[Fe(CN)_{6}]+2\,CaCO_{3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/446d8f669e002bc4b3fa1d31655ecdd9e47dc148)
![{\displaystyle {6\,HCN+FeCl_{2}+4\,KOH{\xrightarrow[{}]{T}}K_{4}[Fe(CN)_{6}]+2\,HCl+4\,H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/46d661698d108b42406750528407c9b00f5c2eb7)
![{\displaystyle {2\,K_{4}[Fe(CN)_{6}]+Cl_{2}{\xrightarrow[{}]{T}}2\,K_{3}[Fe(CN)_{6}]+2\,KCl}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5d4ec06b3932c6c52883fd77c9bc1e6462309c6c)
![{\displaystyle {K_{4}[Fe(CN)_{6}]{\xrightarrow[{}]{T}}4\,KCN+{\underset {fera\,karbido}{FeC_{2}}}+N_{2}\uparrow }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1bae012029bdcb00b37b6e8d11b7d8eb340a4190)
![{\displaystyle {K_{4}[Fe(CN)_{6}]+H_{2}SO_{4}+H_{2}O{\xrightarrow[{}]{T}}K_{2}SO_{4}+FeSO_{4}+(NH_{4})_{2}SO_{4}+CO\uparrow }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0112ad4acc06b00c1f0bada921b6e6810ee276dd)
![{\displaystyle {K_{4}[Fe(CN)_{6}]+H_{2}SO_{4}+KMnO_{4}{\xrightarrow[{}]{T}}KHSO_{4}+{\underset {ferika\,sulfato}{Fe_{2}(SO_{4})_{3}}}+{\underset {mangana\,sulfato}{MnSO_{4}}}+CO_{2}+H_{2}O}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/22845a4b73492b21011caaa401f7849d63b1c35b)
![{\displaystyle {K_{4}[Fe(CN)_{6}]+4\,AgNO_{3}{\xrightarrow[{}]{T}}Ag_{4}[Fe(CN)_{6}]+4\,KNO_{3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f8bc5660e46b0f0f45430117acaa22533f0baa14)
![{\displaystyle {K_{4}[Fe(CN)_{6}]+2\,CuSO4{\xrightarrow[{precipita{\hat {j}}o}]{brunkolora}}Cu_{2}[Fe(CN)_{6}]\downarrow +2\,K_{2}SO_{4}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/22b350f8ea92f3a400791650482056ed4c52fa20)
![{\displaystyle {3\,K_{4}[Fe(CN)_{6}]+4\,FeCl_{3}{\xrightarrow[{precipita{\hat {j}}o}]{blukolora}}Fe_{4}[Fe(CN)_{6}]_{3}\downarrow +12\,KCl}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/49462e2b62b8fd8e4844530228d115a4a0a7efc1)
