Kalia tetrafluoroborato
Aspekto
(Alidirektita el Kalia kvarfluoroborato)
| Kalia tetrafluoro-borato | ||||
 | ||||
| Plata kemia strukturo de la Kalia tetrafluoro-borato | ||||
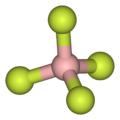  | ||||
| Tridimensia kemia strukturo de la Kalia tetrafluoro-borato | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 14075-53-7 | |||
| ChemSpider kodo | 24637 | |||
| PubChem-kodo | 518872 | |||
| Merck Index | 15,7804 | |||
| Fizikaj proprecoj | ||||
| Aspekto | blanka aŭ cindrokolora solidaĵo | |||
| Molmaso | 125902 g·mol-1 | |||
| Denseco | 2.505g cm−3[1] | |||
| Fandpunkto | 530 °C[2] | |||
| Refrakta indico | 1,3245[3] | |||
| Solvebleco | Akvo:4.4 g/L | |||
| Mortiga dozo (LD50) | 464 mg/kg (buŝe) | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R34 | |||
| Sekureco | S45 S36/37/39 S25 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H314, H319, H335, H413 | |||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P271, P273, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P312, P321, P337+313, P363, P403+233, P405[4] | |||
(25 °C kaj 100 kPa) | ||||
Kalia tetrafluoro-borato estas neorganika kombinaĵo de kalio, fluoro kaj boro, blanka substanco, nesolvebla en akvo kaj kalia fonto por uzoj en oksigen-sensivaj aplikoj, tiel kiel metalproduktado. En koncentriĝoj treege malaltaj, fluoridaĵoj trovas uzon por la traktado de sano.
Fluoraj komponaĵoj povas ankaŭ signifoplenajn uzojn en sintezo de organika kemio. Kutime, ili estas uzataj en metal-alojoj kaj por optikaj deponadoj. Kelkaj fluoraj kombinaĵoj povas esti produktataj laŭ nanoskalaj formoj kaj kun alta pureco. La produktado en alta pureco plibonigas kaj la optikan kvaliton kaj la utileco kiel sciencaj normoj.
Sintezo
[redakti | redakti fonton]- Fluoroborato de kalio estiĝas per traktado de kalia karbonato kun borata acido kaj fluorida acido en du etapoj:
|
2 B(OH)3 + 8 HF → 2 HBF4 + 6 H2O
2 HBF4 + K2CO3 → 2 KBF4 + H2CO3 |
Reakcio
[redakti | redakti fonton]- Sub hejtado, kalia fluoroborato malkomponiĝas en kalia fluorido kaj bora trifluorido:[5]
|
|
Literaturo
[redakti | redakti fonton]- American Elements
- BG RCI Toxicological Evaluations
- Chemicalland21
- Kester Arkivigite je 2017-10-30 per la retarkivo Wayback Machine
- Purification of Laboratory Chemicals
Referencoj
[redakti | redakti fonton]
| ||||||








