El Vikipedio, la libera enciklopedio
Kaliamido
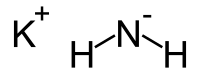
Plata kemia strukturo de la Kaliamido
Tridimensia kemia strukturo de la Kaliamido
Alternativa(j) nomo(j)
Amido de kalio
Potasamido
Kemia formulo KNH2
CAS-numero-kodo 17242-52-3
ChemSpider kodo 78490
PubChem-kodo 87015
Fizikaj proprecoj
Aspekto flaveca solidaĵo
Molmaso 55,121 g·mol−1
Denseco 1,57g cm−3
Fandpunkto 338 °C
Solvebleco Akvo :reakcias
Mortiga dozo (LD50) 187 mg/kg (buŝe)
Sekurecaj Indikoj
Riskoj R14 R19 R29 R34 R50
Sekureco S6 S7/8 S26 S36/37/39 S45 S61
Pridanĝeraj indikoj
Danĝero
GHS Damaĝo Piktogramo
GHS Signalvorto Damaĝa substanco
GHS Deklaroj pri damaĝoj H261 , H314 , H400
GHS Deklaroj pri antaŭgardoj P231 , P232 , P273 , P280 , P305+351+338 , P310 , P422
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo25 °C kaj 100 kPa)
Kaliamido aŭ KNH2 estas neorganika komponaĵo konsistante je kalia katjono (K+ ) kaj konjugata bazo de amoniako (NH2 )- . Ĝi estas flavo-bruna solidaĵo uzata kiel kemia reakcianto kun alkalaj proprecoj.
2
K
+
2
N
H
3
→
65
−
105
o
C
2
K
N
H
2
+
H
2
{\displaystyle {\mathsf {2\ K+2\ NH_{3}{\xrightarrow {65-105^{o}C}}2\ KNH_{2}+\ H_{2}}}}
K
H
+
N
H
3
→
300
o
C
K
N
H
2
+
H
2
{\displaystyle {\mathsf {KH+NH_{3}{\xrightarrow {300^{o}C}}\ KNH_{2}+H_{2}}}}
K
2
O
+
N
H
3
→
−
50
o
C
K
N
H
2
+
K
O
H
{\displaystyle {\mathsf {K_{2}O+NH_{3}{\xrightarrow {-50^{o}C}}\ KNH_{2}+KOH}}}
Kiam submetita al varmigo, kaliamido malkomponiĝas:
6
K
N
H
2
→
600
o
C
6
K
+
4
N
H
3
+
N
2
{\displaystyle {\mathsf {6\ KNH_{2}{\xrightarrow {600^{o}C}}\ 6\ K+4\ NH_{3}+N_{2}}}}
K
N
H
2
+
H
2
O
→
K
O
H
+
N
H
3
{\displaystyle {\mathsf {KNH_{2}+H_{2}O{\xrightarrow {\ }}\ KOH+NH_{3}}}}
Kaliamido reakcias kun ne-oksidigaj acidoj:
K
N
H
2
+
2
H
C
l
→
K
C
l
+
N
H
4
C
l
{\displaystyle {\mathsf {KNH_{2}+2\ HCl{\xrightarrow {\ }}\ KCl+NH_{4}Cl}}}
Ĝi reakcias kun oksidigaj acidoj:
2
K
N
H
2
+
2
H
N
O
3
→
K
N
3
+
K
N
O
3
+
3
H
2
O
{\displaystyle {\mathsf {2\ KNH_{2}+2\ HNO_{3}{\xrightarrow {\ }}\ KN_{3}+KNO_{3}+3\ H_{2}O}}}
K
N
H
2
+
N
H
4
C
l
→
−
40
o
C
/
l
i
k
v
a
a
m
o
n
i
a
k
o
2
N
H
3
↑
+
K
C
l
{\displaystyle {\mathsf {KNH_{2}+NH_{4}Cl{\xrightarrow {-40^{o}C/likva\,amoniako}}\ 2\,NH_{3}\uparrow +KCl}}}
K
N
H
2
+
A
s
H
3
→
K
A
s
H
2
h
i
d
r
i
d
o
d
e
k
a
l
i
o
k
a
j
a
r
s
e
n
o
+
N
H
3
{\displaystyle {\mathsf {KNH_{2}+AsH_{3}{\xrightarrow {}}\ {\underset {hidrido\,de\,kalio\,kaj\,arseno}{KAsH_{2}}}+NH_{3}}}}
Potasamido reakcias kun piridino por doni 2-amino-piridinon [ 3]
Potasamido reakcias kun tiofeno por doni 2-amino-tiofenon :
Potasamido reakcias kun benzoila klorido por doni benzamido :
Amido de kadmio estas blanka pulvoro kiu eksplodas sub rapida varmigo. Ĉi-salo povas prepariĝi per traktado de la kadmia jodido aŭ cianido de kadmio kun potasamido en ĉeesto de likva amoniako [ 4]
C
d
I
2
+
2
K
N
H
2
→
C
d
(
N
H
2
)
2
+
2
K
I
{\displaystyle {\mathsf {CdI_{2}+2\,KNH_{2}{\xrightarrow {}}Cd(NH_{2})_{2}+2\,KI}}}
Potasamido reakcias kun kloro-benzeno por doni anilinon :
Neorganikaj saloj de kalio




















![{\displaystyle {\mathsf {{\xrightarrow[{100^{o}C-130^{o}C}]{likva\,amoniako}}\ }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7f63067603a0c5dc7292fc1c5b857bb7386aaa10)



![{\displaystyle {\mathsf {{\xrightarrow[{}]{likva\,amoniako}}\ }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/24c7eb4584e8f617dba7a7e9afe35ccce0712f95)